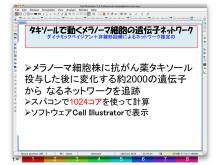
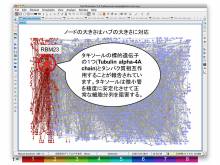
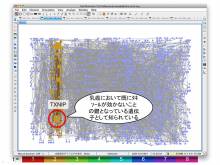
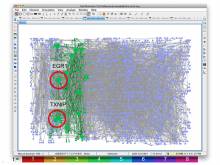
システムがんアウトリーチ 「名古屋大学医学部鶴舞祭」2011年6月11日~12日
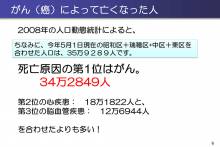
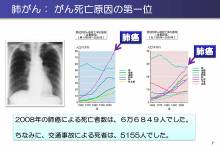
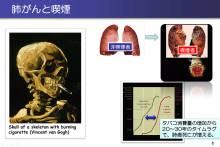
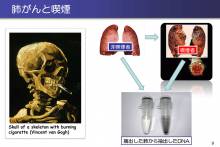
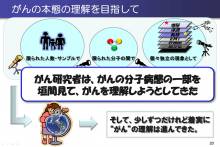
がんとスーパーコンピュータ!
名古屋大学医学部の高橋隆です。
スライド
東京大学医科学研究所ヒトゲノム解析センターの宮野悟です。
スライド
プロテオーム解析の実験室の見学
次は遺伝子発現を調べるマイクロアレイ解析の実験室の見学です
参加者の感想
参加人数:6月11日(土)20人(満員)、6月12日(日)14人
- 講座は面白かったですか?
- 面白かった 11人
- やや面白かった 4人
- やつまらなかった 0人
- つまらなかった 0人
- 医学・医療に対する関心は高まりましたか?
- 高まった 13人
- 変わらない 2人
- 講座の感想を教えてください。
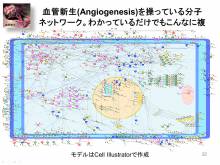
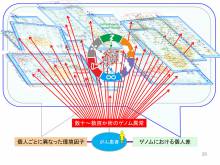
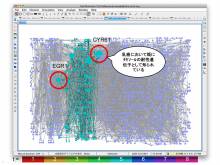
- ゲノム解析後の応用で、全遺伝子を一度に調べる方法としてネットワークの考え方が利用されていることがよくわかり、この解析にスーパーコンピュータが必要なことが良く分かった。
- 医学部の講座(鶴舞)にははじめて来ました。最新のことにふれられて面白かったです。ありがとうございました。スーパーコンピュータでの解析、頑張ってください。
- 数学と医学の合体は新たな扉を開くいいきっかけになりそう。
- 基礎学問の重要性が理解できた。又、地道な基礎研究により、進歩があることも合わせて理解できた。
- 大変勉強になった。最新の情報を得ることができた。
- ヒトゲノムの個人差について等、日頃疑問に思っていたことに関する話が聞けて、大変参考になりました。ありがとうございました。
- 環境的因子・要因の研究もあれば聞きたかった。環境的因子と疾患の因果関係を知りたいと思いました。
- 数学的手法でガンの治療方法を模索するということを解りやすく説明して下さり、ありがとうございました。
- 医学が日進月歩だとは、昔からよく言われていることですが、10年逃げ切れば(健康でいれば)長生きできそうですね。遺伝子とタンパク質の解析は文章でよく読みますが、初めて見ることができイメージできました。例えがわかりやすくておもしろかったです。
- ガンの研究を見せてもらって、やりがいが有ると思いました。
- 専門的なことを学生にもわかるように簡単に教えてくれた。機材って高い。
- 非常に解りやすく、面白い講座でした。多少専門用語も多かったのは少し気になります。あと、1時間の延長で塾に遅れそうです。
- 専門的なことを解りやすく説明してもらったり、実際の機材を見せてもらったら、とても楽しく勉強になりました。
- スーパーコンピュータの力の凄さがちょっとわかりました。分子腫瘍学の先生がとても分かり易かったと思います。もっと予算がついたら良いと思いますが、頑張ってください。